随着欧盟及其它很多国家在化妆品领域中施行动物实验禁令以及3R理念的普及, 使用非动物测试手段开展化妆品及化学品的安全评估一直是个热门研究领域。以前我们把这些非动物测试手段(比如体外试验)叫做替代测试方法(Alternative Test Methods),然而这个名字逐渐被新技术方法(New Approach Methodologies,简称NAM)这个新词汇所替代。从事NAM研究的学者也越来越多,NAM早已成为毒理及法规科学会议上的明星嘉宾。对从事毒理及安全评估的法规及技术人员而言,仿佛不知道NAM就落后了一个时代。本文将详细介绍什么是新技术方法 (NAM),它与替代测试方法的区别以及NAM包含了哪些安全评估技术与方法。
什么是新技术方法(NAM)?
新技术方法 (NAM)被定义为可通过避免使用完整动物进行测试而提供化学品危害和风险评估信息的任何技术、方法或其组合。它的定义很广,包括计算机模拟评价(in silico)、体外化学分析法(in chemico)和体外试验(in vitro)方法。它还包括各种新的测试工具,如“高通量筛选”和“高含量筛选”,如基因组学、蛋白质组学、代谢组学以及一些改进的“传统”方法。
新技术方法 (NAM)听上去像学者们的谈资,但实际上早已被欧美管理部门比如欧盟ECHA、欧盟EFSA和美国EPA纳入到化学品危害评估、风险评估和管理决策中去了。通过新技术方法 (NAM)减少或替代动物测试已是大势所趋。在未来,新技术方法 (NAM)大概率会成为提供化学品危害及风险信息的首要手段。
新技术方法(NAM)与替代测试方法有什么区别?
传统的动物替代测试方法实际上包括体外试验方法和改良的体内试验方法(比如使用动物数量更少),但它们有个共同点, 都是基于”测试“的方法。新技术方法 (NAM)显然范围更广,还包括了很多非”测试”方法,比如计算机模拟、交叉参照(read-across)和毒理学阈值关注(TTC)。除此以外,新技术方法 (NAM)不仅仅是替代动物测试而已,它本身就包含了很多新的毒理研究领域,比如有害结局通路(Adverse outcome pathway, AOP)。
接下来我们就看看新技术方法 (NAM)到底包含哪些常用手段和方法。
计算机模拟实验(in silico)
借助数学模型, 人工智能等先进的计算机辅助手段, 科学家们可以利用统计学, 生物学科, 化学, 物理等基础学科知识, 分析相关毒理学测试实验数据, 从而预测化学品的毒性数据以及在环境中的暴露浓度,为化学品的风险评估提供关键信息。
定量构效关系(QSAR)
Quantitative Structure-Activity Relationship(简称“QSAR”),使用数学模型来描述分子结构和分子的某种生物活性之间的关系,基本假设为化合物的活性与其结构相关。从各种分子描述符出发,通过模型算法,即可预测相关的理化性质,生物学活性,毒理学效应,环境行为和归趋等特性。一般而言,在使用QSAR模型时,选择合适的、预测性能好、被验证过的模型去预测未知化合物的某种生物活性,显得尤为关键,且不同模型或方法获得的生物活性结果之间可以相互验证最为理想,同时必须确定该物质应属于QSAR模型的适用范围。
常见QSAR模型 (免费)有OECD QSAR Toolbox, Toxtree,EPI Suite,这些免费模型软件基本可以满足日常使用需求。
物质分组(Grouping/Category)和交叉参照法(READ-ACROSS)
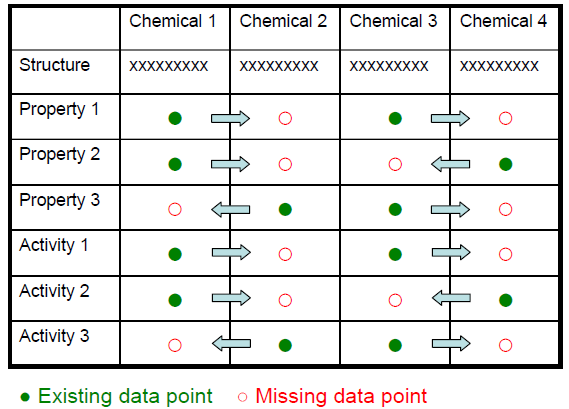
利用了结构相近、性质相似的原理,将某些由于结构相似而遵循某个规则的物质,归为一组(group),或一“类”(category)。通过在组内插入其他参考物质,利用“组”内各参考物质的现有数据,通过交互参照的方式(READ-ACROSS),预测其他物质缺失的理化、毒理或生态毒理性质,从而避免每种物质的每个性质进行测试的需求,节约数据成本。
毒理学阈值关注(TTC)
毒理学关注阈值(TTC)的原理是可以对一般化学物质建立一个通用的暴露阈值(这个阈值与化学物质结构有关), 当化学物质的人体暴露剂量低于这个阈值水平时,该化学物质对人体健康造成负面影响的可能性很小(即使没有这个化学物质的毒性数据)。
TTC方法主要用于评估化学结构明确、缺乏详尽毒理学数据且对人体暴露量低的化学物质的风险,常用于香精香料、食品、化学原料及产品中杂质或微量添加物的风险评估。
在使用TTC方法前首先要确定该方法是否适用于目标物质的评估(TTC方法不适用于无机物,有生物蓄积性的物质和纳米材料等)。然后根据Cramer决策树确定Cramer结构分类并选取如下暴露阈值用于风险评估(假设人均体重60kg)。
- Cramer I类:30 µg/kg bw/d
- Cramer II类:9 µg/kg bw/d
- Cramer III类:1.5 µg/kg bw/d
- 有机磷酸酯类:0.3 µg/kg bw/d
- 对于有遗传毒性预警的物质:0.15 µg/kg bw/d
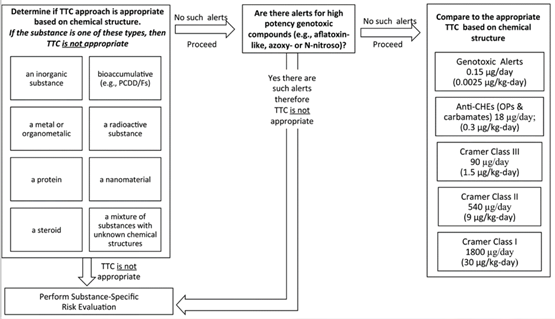
可以协助判断Cramer结构类别的软件有ToxTree和OECD QSAR Toolbox等。TTC完整流程评估方法如下所示:
有害结局通路(Adverse outcome pathway, AOP)
在传统动物毒性试验中我们通常观察记录动物的死亡、突变、器官损伤、肿瘤等终点,然而这些有害结局(Adverse outcome)实际上都是起始于细胞/分子层面对暴露化合物的反应。毒性通路就是对从细胞层面分子起始事件(Molecular Initiating Event, MIE)到有害结局这一连续细胞反应和关键事件(Key Event, KE)的描述说明。比如化合物暴露引起的分子起始事件首先造成一系列的蛋白水平的级联反应如受体蛋白的激活,随后引发一系列关键事件比如促进某些酶的合成、细胞的增殖或死亡等,最终导致组织或器官的损伤或个体死亡甚至种群的改变。
验证过的毒性通路中各个事件一般是可以验证识别或可检测的,同时它们之间的发生应具有可靠的因果关系。对于已建立且被验证过的毒性通路,我们只需要对通路中的分子起始事件和关键毒性事件展开试验即可推断出最终的毒性损伤效应,从而避免高级别的耗时费力的动物实验。检测低层次(分子或细胞水平)的毒性事件通常可以使用体外或离体试验技术开展,费用低、周期短、通量高,与传统的动物毒性试验相比有明显优势。
不过目前已经验证过的毒性通路比较有限, 且建立新的毒性通路技术难度大,目前基于毒性通路的测试策略尚不能替代传统动物试验。
小结
新技术方法 (NAM) 的定义很广泛,同时包括了测试手段和非测试方法,可以通过避免使用完整动物进行测试而提供化学品危害和风险评估信息。本文所提到常用技术有些并不能称为真正的“新”, 但这个领域的发展是日新月异的,很多新技术比如高通量筛选、基因组学、蛋白组学和有害结局通路说不定有天会彻底改掉我们对动物试验的依赖。
来源:瑞旭集团
作者:张霄鹏、石云波

