一、2021年化妆品新原料备案数据分析
自2020年6月29日《化妆品监督管理条例》(国令第727号)发布以来,一系列的配套法规相继推出,其中与化妆品新原料注册备案相关的新法规文件包括《化妆品注册备案管理办法》、《化妆品新原料注册备案资料管理规定》及《化妆品安全评估技术导则》等。2021年5月1日起,化妆品新原料注册备案需在国家药品监督管理局网上办事大厅的化妆品智慧申报审评系统中进行申请。
自新法规实施以来,2021年5月1日至2022年1月24日期间,共有7个化妆品新原料通过备案。其中5个属于国产化妆品新原料(具体信息详见表1),2个属于进口化妆品新原料(具体信息详见表2)。瑞旭集团日化团队成功协助两家原料企业完成首个进口新原料和第2个进口新原料的备案。
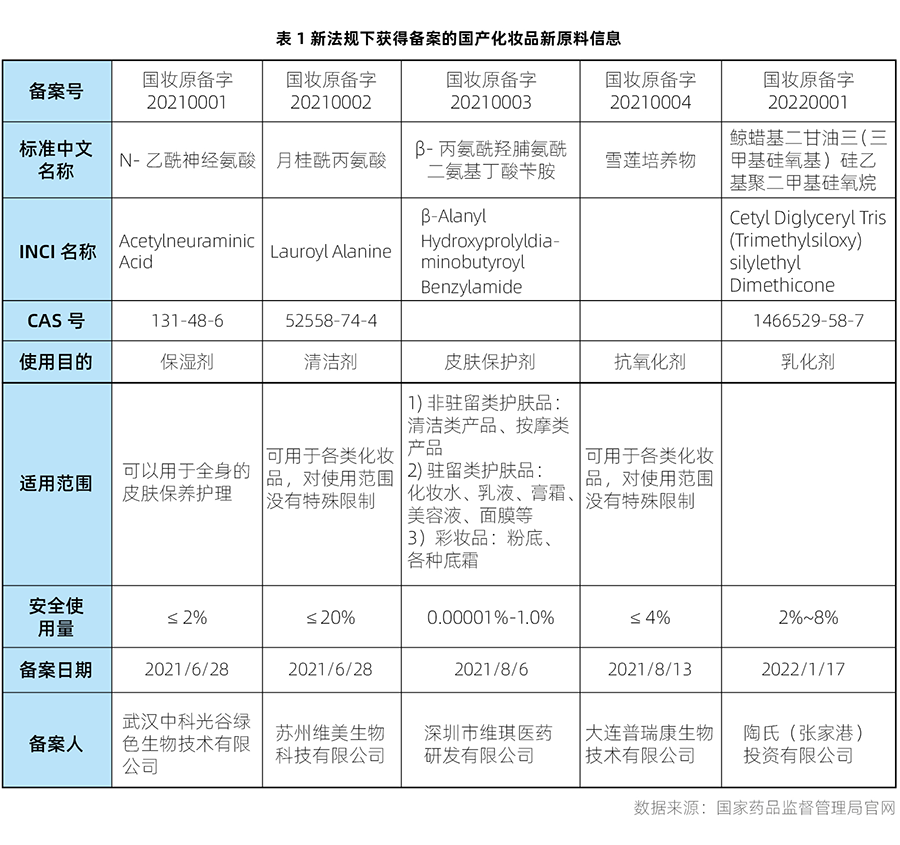
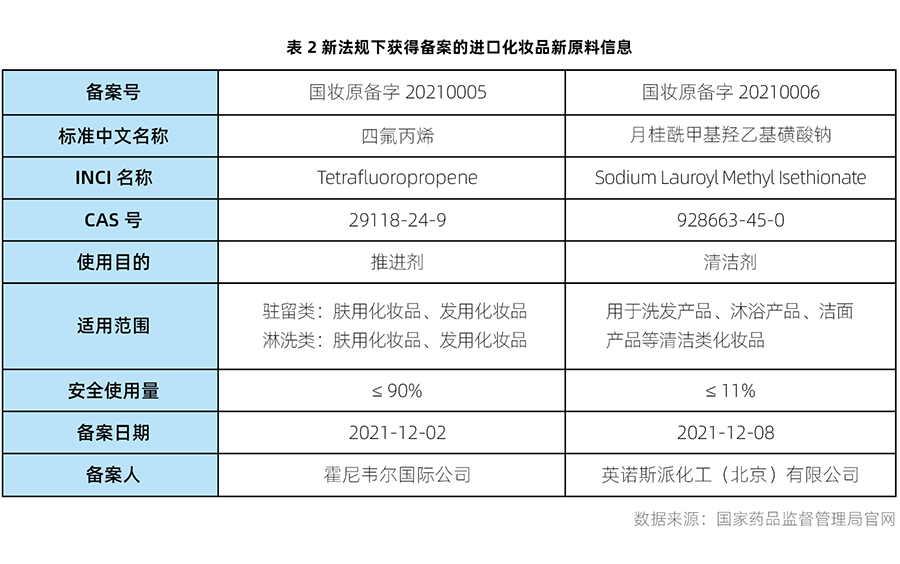
根据2021年4月23日中国食品药品检定研究院发布关于化妆品新原料过渡期处理细则的公告,对原化妆品行政许可系统已受理尚未作出行政许可决定的化妆品新原料有两种处理方式:
1)申请人可于2021年5月1日前提出撤回行政许可申请,办理申报资料退回手续;
2)申请人未按期提出撤回行政许可申请的,自2021年5月1日起,中检院拟按照《化妆品新原料注册备案资料管理规定》的资料要,求继续完成审评审批工作。
上表中通过备案的3个化妆品新原料来自原化妆品行政许可系统已受理尚未作出行政许可决定的化妆品新原料(共计37件)。
根据《化妆品注册备案管理办法》第二章化妆品新原料注册和备案管理第十二条:调整已使用的化妆品原料的使用目的、安全使用量等的,应当按照新原料注册、备案要求申请注册、进行备案。表明在使用已备案的化妆品新原料过程中,其使用目的、适用范围以及安全使用量需参照公布的备案信息。如果信息有更新或调整需按照新原料注册备案要求重新进行申请。
二、旧法规体系下化妆品新原料注册数据分析
在旧法规《化妆品卫生监督管理条例》下,从2004年至2021年5月1日前,一共批准了14个新原料(具体信息详见表3)。
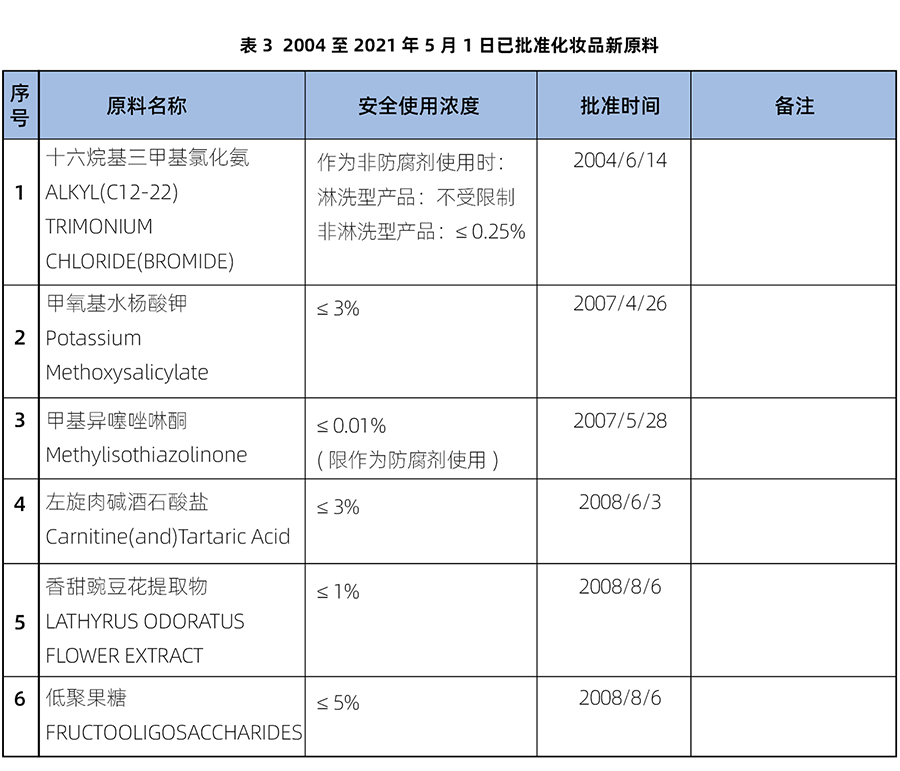
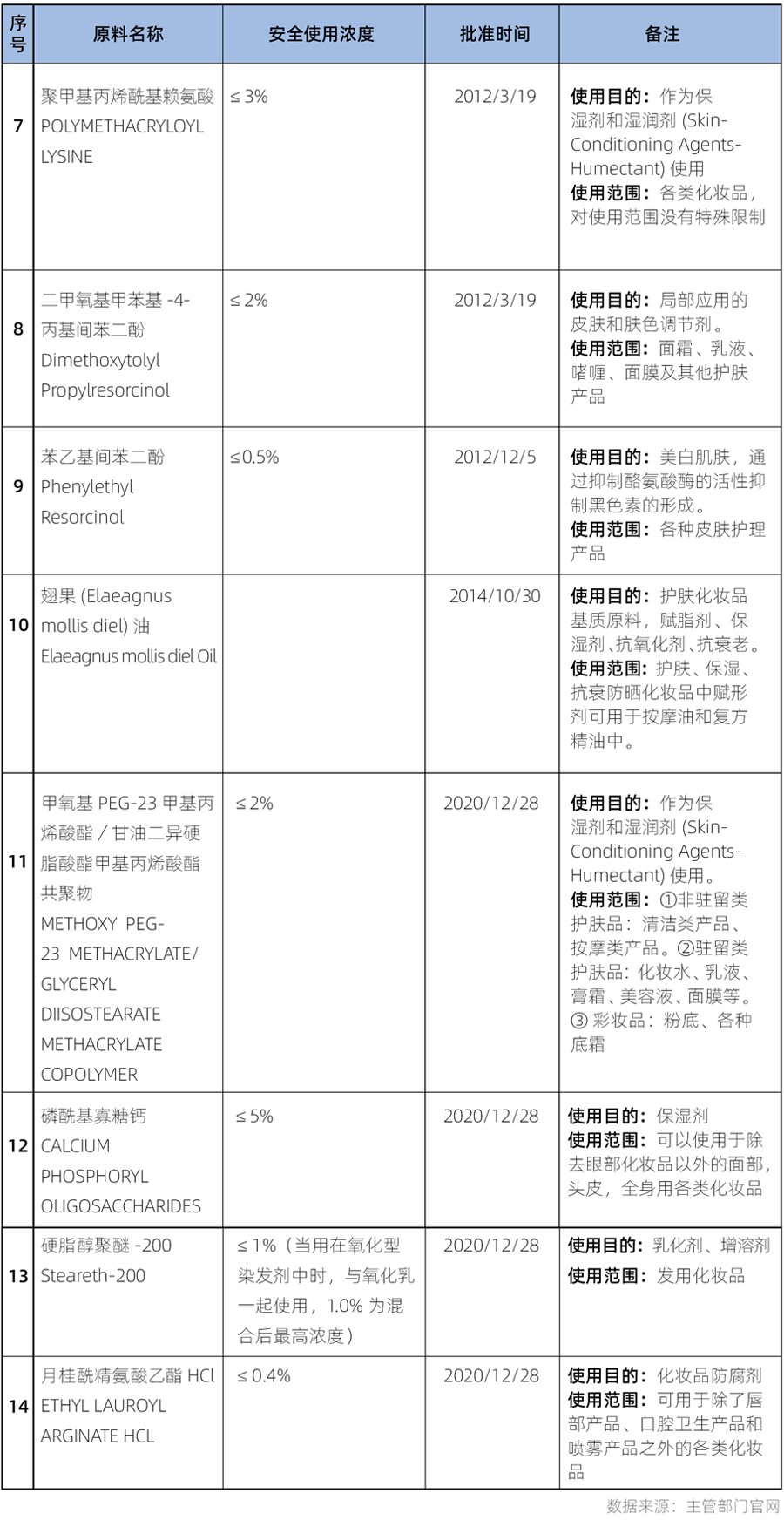
上表中1-6号原料由原卫生部批准,7-10号原料由原国家食品药品监督管理(总)局批准,11-14号由国家药品监督管理局批准。这些原料的审批过程也见证了有关国家机构的变迁和更迭。2008年9月化妆品的卫生行政许可工作由卫生部移交至国家食品药品监督管理局。2013年3月22日,国家食品药品监督管理局(State Food and Drug Administration,简称SFDA)改名为国家食品药品监督管理总局(China Food and Drug Administration,简称CFDA。2018年4月10日,国务院机构改革中原“国家食品药品监督管理总局”也正式变更为“国家药品监督管理局”)。
三、中国化妆品新原料法规发展进程
● 1989年《化妆品卫生监督管理条例》
根据《化妆品卫生监督管理条例》第九条,使用化妆品新原料生产化妆品,必须经国务院卫生行政部门批准。化妆品新原料是指在国内首次使用于化妆品生产的天然或人工原料。
● 2011年《化妆品新原料申报与审评指南》
该文件于2011年7月1日实施。其中包括化妆品新原料定义、安全性要求、申报资料要求、审评原则。
● 2011年关于进一步规范化妆品新原料行政许可有关事项的通知
该通知对毒理学实验开展前的数据要求以及毒理学实验报告要求等内容进行了阐述。
● 2015年国家食品药品监督管理总局关于发布已使用化妆品原料名称目录(2015版)的通告
依据《化妆品卫生监督条例》等有关规定,国家食品药品监督管理总局对2014年6月30日发布的已使用化妆品原料名称目录进行了调整更新,形成了已使用化妆品原料名称目录(2015版)。目录收录了8783个化妆品原料。该目录作为判断是否属于化妆品新原料的依据。
● 2020年《化妆品监督管理条例》
根据《化妆品监督管理条例》第四条,化妆品原料分为新原料和已使用的原料。国家对风险程度较高的化妆品新原料实行注册管理,对其他化妆品新原料实行备案管理。根据《化妆品监督管理条例》第十一条,在我国境内首次使用于化妆品的天然或者人工原料为化妆品新原料。具有防腐、防晒、着色、染发、祛斑美白功能的化妆品新原料,经国务院药品监督管理部门注册后方可使用;其他化妆品新原料应当在使用前向国务院药品监督管理部门备案。国务院药品监督管理部门可以根据科学研究的发展,调整实行注册管理的化妆品新原料的范围,经国务院批准后实施。
● 2021年国家药监局关于发布《已使用化妆品原料目录(2021年版)》的公告
依据《化妆品监督管理条例》相关规定,国家药监局组织对《已使用化妆品原料目录名称(2015版)》进行修订,形成了《已使用化妆品原料目录(2021年版)》,现予公布,自2021年5月1日起施行。目录收录8972个化妆品原料。
● 2021年《化妆品新原料注册备案资料管理规定》
涵盖化妆品新原料注册备案资料要求内容。
● 2021年关于化妆品新原料过渡期处理细则的公告
针对原化妆品行政许可系统已受理尚未作出行政许可决定的化妆品新原料的处理方式。
● 2021年国家药监局关于试行化妆品电子注册证的公告
自2022年1月1日起,按照《化妆品注册备案管理办法》提出申请并获准注册的特殊化妆品和化妆品新原料,开始发放电子注册证。
四、新旧监管体制比较
在过去旧监管体系下,化妆品新原料审批难、审批慢的原因主要表现在以下几个方面:
1. 前期无统一的参考目录判定是否属于新原料;
2. 由于《化妆品卫生监督条例》未对新原料进行细化分类,新原料的申报要求较高,《化妆品新原料申报与审评指南》的资料要求没有进行细化说明,造成技术审评过程中存在专家与企业对审评要求理解不一致、原料生产商为保护商业秘密不愿意提供足够的信息等问题;
3. 化妆品原料管理体系较不完善,比如批准后的新原料如何监管;通常启动一个化妆品新原料项目,瑞旭集团日化团队都会建议企业做好五年以上的准备。批准的新原料通过公告形式对外公示,意味着所有企业可以直接生产和/或使用批准的新原料。这样的管理方式难以鼓励原料生产商开展新原料申请,不利于促进化妆品产业创新;
4. 动物实验数据的强制要求与2013年欧盟全面禁止动物实验的化妆品法规相违背,使得很多进口尤其欧洲化妆品新原料项目难以启动或中途夭折;
5. 无对外交流窗口可以直接与审评专家沟通讨论审评意见;
6. 美容产业技术创新的必要性不及药品和食品产业。
在新监管体系下,化妆品新原料管理变化主要表现在:
1. 化妆品新原料根据风险程度进行分级管理,取代旧监管体系下的“一刀切”方式,对待高风险的化妆品新原料基本保留了原有管理模式。而对于非高风险的化妆品新原料采取备案制,大大缩短了官方审评时间。依据瑞旭集团日化团队经验,旧监管体系下的化妆品新原料项目周期约一半以上的时间徘徊在资料补充和技术审评环节;
2. 相较2011年7月1日实施的《化妆品新原料申报与审评指南》,今年5月1日实施的《化妆品新原料注册备案资料管理规定》无疑更加完善和明晰了化妆品注册备案资料要求。新监管体系下的化妆品注册备案资料要求与旧监管体系相比没有减少反而有所增加,比如增加了功效依据资料、安全使用历史相关资料等;
3. 《化妆品新原料注册备案资料管理规定》中明确了动物替代方法要求。意味着“动物替代方法”的大门终于向化妆品新原料打开,只是对于未收录于《化妆品安全技术规范》的动物替代试验方法需要确认其是否已被国际权威替代方法验证机构收录,且需要提交该方法能准确预测该毒理学终点的证明资料。虽然国内的动物替代方法在逐步完善,但目前已经接受的替代方法仍然有限,导致新法规实施前期对很多国际化妆品原料企业来说,动物实验数据依然成为化妆品新原料项目推进的阻力之一;
4. 对于一些非高风险的功能性新原料如防脱发、祛痘、抗皱(物理性抗皱除外)、去屑、除臭功能,虽然按照备案制管理,但其毒理实验要求同高风险新原料仍然保持一致;
5. 细化毒理实验情形,比如只有针对国内外首次使用的有健康危害效应(不包括局部毒性)的新原料才要求开展毒物代谢及动力学试验;对于国内外首次使用的高风险的新原料、较高生物活性的新原料、纳米新原料,需要考虑长期人体试用安全试验、皮肤吸收/透皮试验、免疫毒性试验;
6. 毒理安全评估要求参考最新的《化妆品安全评估技术导则(2021年版)》进行制作;
7. 对通过注册备案的新原料设定3年监测期,即在监测期内,新原料注册人或备案人拥有新原料的使用权,每年应定期向国务院药品监督管理部门报告新原料使用和安全情况。
由于旧监管体系下对化妆品新原料没有分类管理,加之审评尺度未结合化妆品原料的特点进行细化,在我国获批的化妆品新原料屈指可数。虽然新监管体系下对化妆品新原料安全性和注册备案资料方面并没有放松要求,但化妆品新原料分级管理制度有利于风险性较小的化妆品新原料通过备案尽早上市,同时对新原料设定3年监测期,即在监测期内,新原料注册人或备案人拥有新原料的使用权,每年应定期向国务院药品监督管理部门报告新原料使用和安全情况。因此,3年安全风险监测期的设置让申请企业的利益获得保障的同时也让企业主动承担起安全风险监测的责任。这无疑大大促进了产业创新与发展。相信在科学监管体系下,化妆品新原料备案的春天已到来。
相关推荐:
我们的服务:

